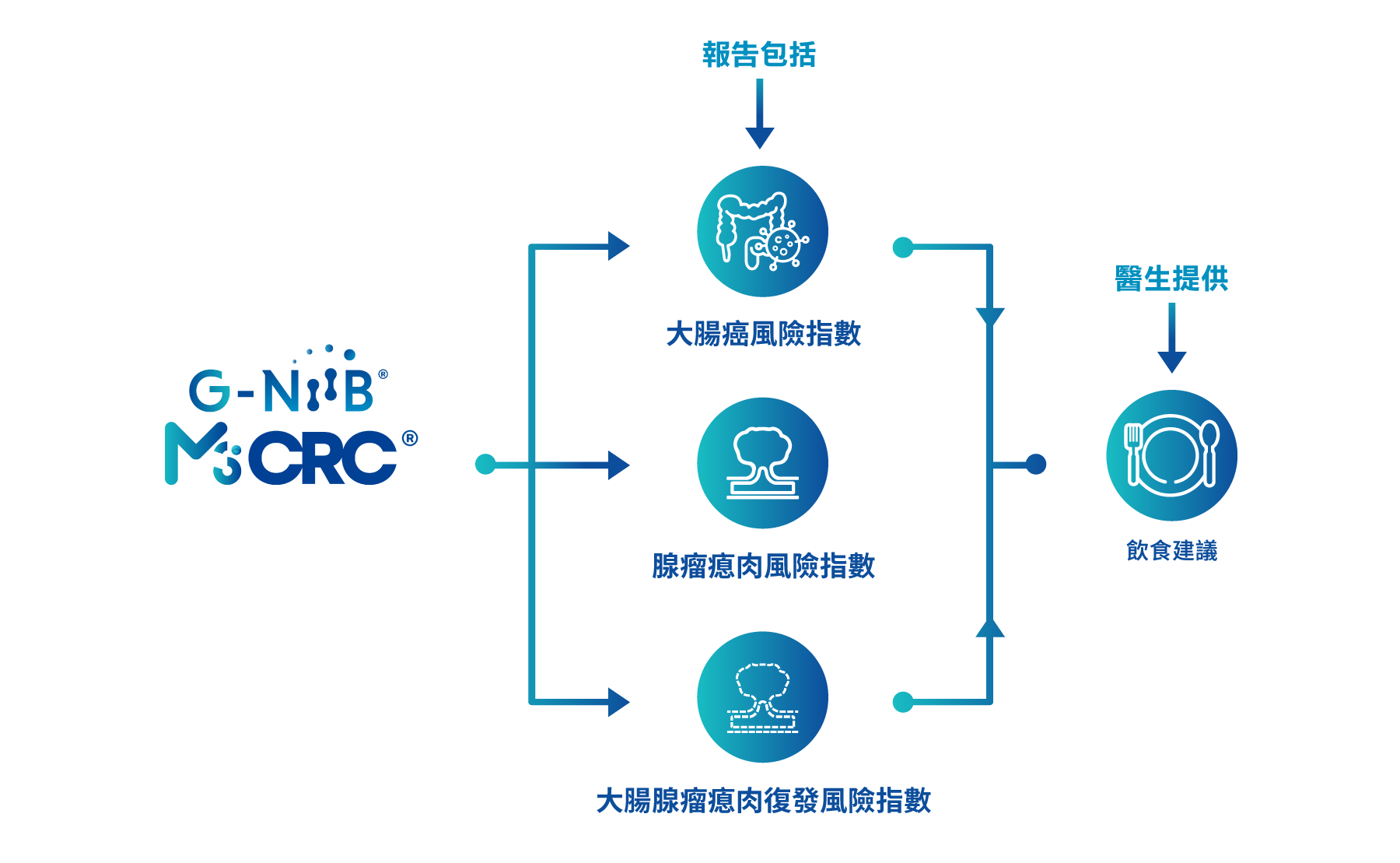
全球首創 M3細菌基因檢測技術
可偵測大腸癌、大小瘜肉及瘜肉復發之
非入侵性大腸癌風險檢測
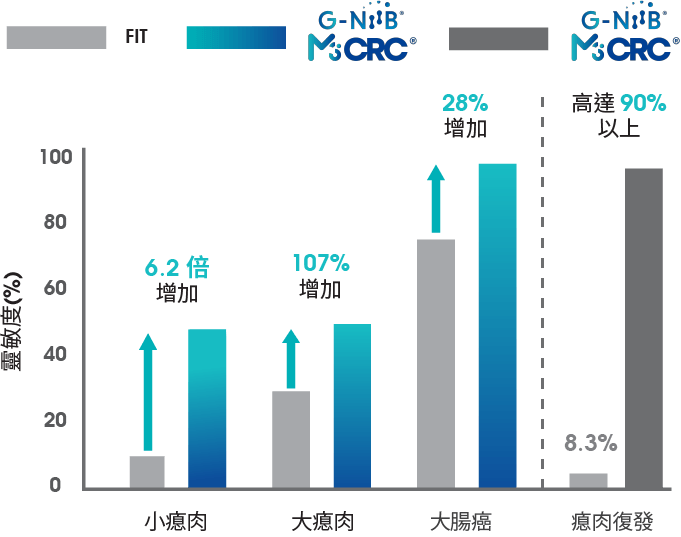
結直腸癌(俗稱大腸癌)自2013年起成為香港頭號癌症,並在致命癌症中排名第二位。研究指出,大部份大腸癌都是由小瘜肉演變而成,因此及早發現大腸瘜肉對於預防大腸癌及改善存活率,有莫大的幫助。但小瘜肉並無癥狀不易察覺,因此需依靠特別的檢測才能偵測到。G-NiiB M3CRC是全球首創的嶄新科研技術,是市面上唯一可偵測大小瘜肉的非入侵性大腸癌風險檢測,而其偵測大腸癌的靈敏度更高達 94%,相當於結腸鏡檢查(大腸鏡)1。
以大便隱血測試(fecal immunochemical test,簡稱FIT)為例, 對小瘜肉的靈敏度只有7.6% 。即使是嶄新的大便DNA測試,對小瘜肉的靈敏度亦只有17.2%9。
(Imperiale, NEJM, 2014)



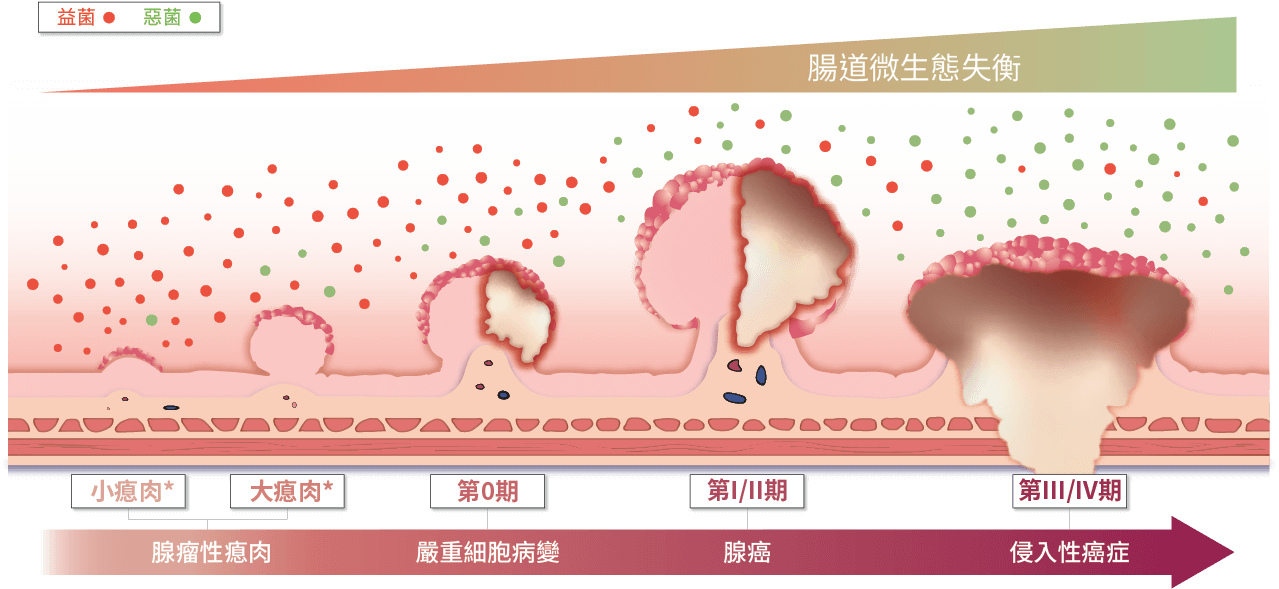
by Yachida et al., Nature Medicine, 2019 and Sporadic (Nonhereditary) Colorectal Cancer: Introduction, by Johns Hopkins Colon Cancer Center. https://www.hopkinsmedicine.org/gastroenterology_hepatology/_pdfs/small_large_intestine/sporadic_nonhereditary_colorectal_cancer.pdf
*小瘜肉指非進展期腺瘤(non-advanced adenoma)
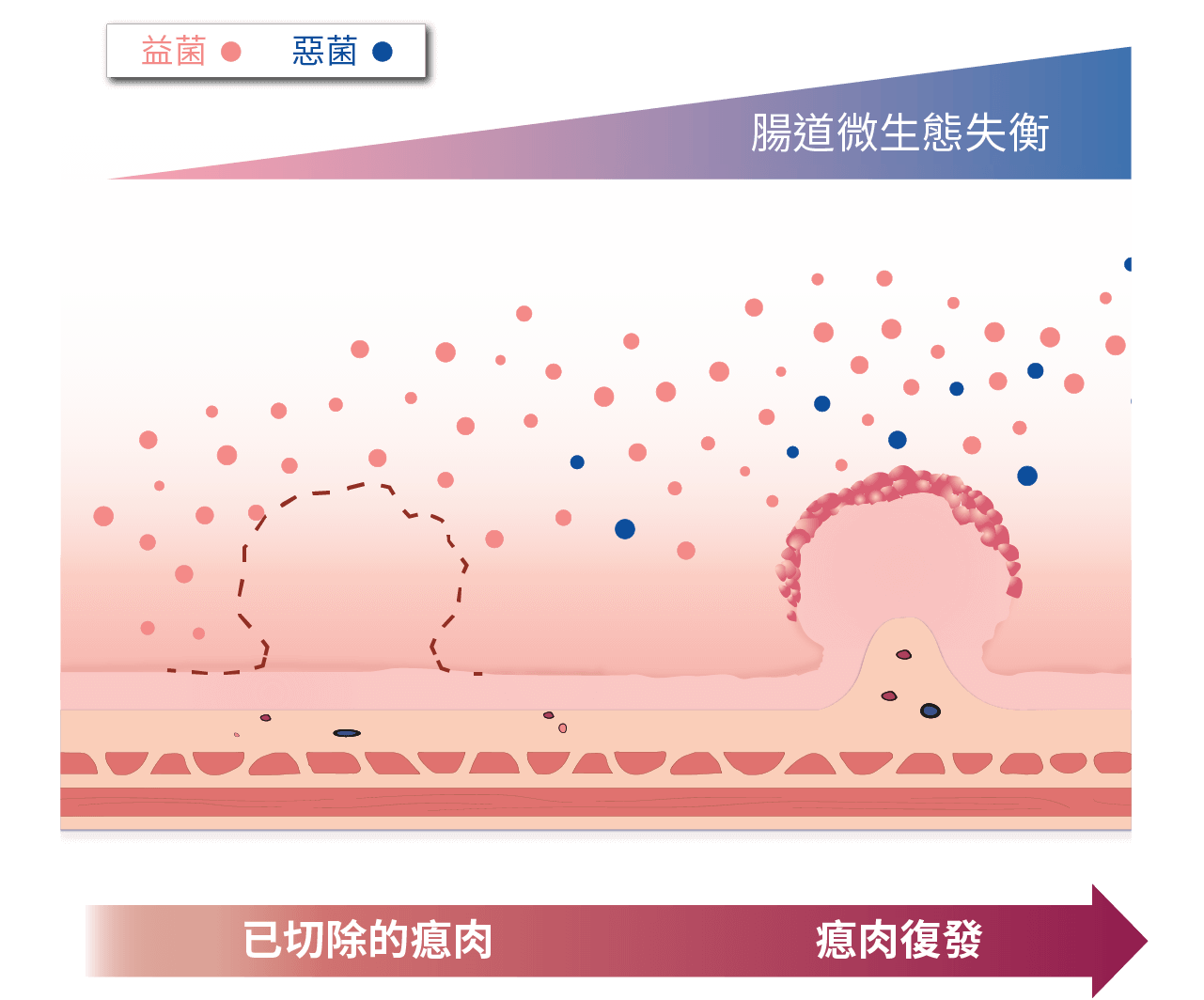
#1. ME Martinez, R Sampliner, JR Marshall, et al. Adenoma characteristics as risk factors for recurrence of advanced adenomas. Gastroenterology 2001;120:1077-83.